研究室紹介OPAL-RING
松田 研究室
記憶や学習の基盤―シナプス可塑性を操る
| 所属 | 大学院情報理工学研究科 先進理工学専攻 |
|---|---|
| メンバー | 松田 信爾 准教授 |
| 所属学会 | 日本生理学会、北米神経科学学会、日本神経科学学会 |
| 研究室HP | http://www.matsuda-lab.es.uec.ac.jp/ |
| 印刷用PDF |
掲載情報は2015年8月現在

- 松田 信爾
Shinji MATSUDA
- キーワード
-
シナプス可塑性、長期抑圧、長期増強、グルタミン酸受容体、エンドサイトーシス、エキソサイトーシス
「記憶」や「学習」は脳の高次機能の代表格としてよく知られています。生物はこの記憶や学習をどのように行っているのでしょうか。今日では多くの神経科学者が、脳の神経細胞間のつなぎ目である「シナプス」の機能や形が強い刺激によって変化し、刺激を除いた後もその痕跡が残るという、あたかも“粘土のような”脳の可塑的性質が働いているからだと考えています。
可塑性とは本来、物が外力を受けるとそれに反応して変形し、その後もその形状が保たれることをいいます。plasticity(可塑性)はギリシャ語に起源を持つ英語ですが、例えば、人工的に有用な形状に作られた「プラスチック」はこれが語源になっています。工業分野では可塑性材料はよく使われます。中枢神経における可塑性とは、外界から入ってきた刺激に対して神経系が構造的、あるいは機能的に変化する性質のことを指します。
松田信爾准教授は、中枢神経系の臓器である脳の「シナプス可塑性」の現象の解明を目指し、これまでに記憶と忘却の脳内メカニズムの鍵をいくつも突き止めてきました。こうした研究を通じて、松田准教授は「記憶や学習障害などの病態の理解や、その治療法の開発に役立たせたい」と考えています。
人間の脳は、膨大な数の神経細胞がシナプスによって結合し、電気信号を次から次へと伝えています。シナプスにおける信号の伝達効率が長期間にわたって増強、または抑圧されることが記憶・学習や忘却過程の仕組みであるとされ、それぞれ「長期増強(Long Term Potentiation:LTP)」、「長期抑圧(Long Term Depres-sion:LTD)」と呼ばれています。
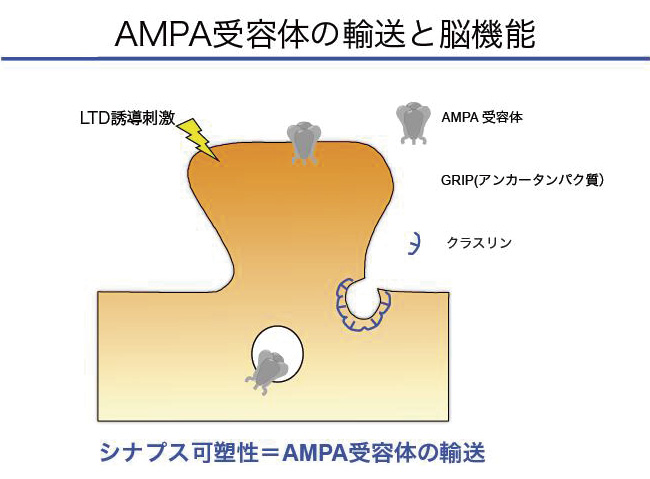
シナプスにおける信号の伝達は神経細胞の表面に存在するAMPA型グルタミン酸受容体(AMPA受容体)が担っており、その伝達効率が状況に応じて変化する現象が「シナプス可塑性」です。LTPやLTDはシナプス可塑性の一種であり、AMPA受容体の数の増減によって起きると考えられています。しかし、LTPおよび、LTDの分子メカニズムは最近まで未解明のままでした。
こうした背景のもとで、松田准教授らの研究チームは、新しい記憶を獲得する過程で重要な脳部位とされる海馬の神経細胞を使って、LTD時にAMPA受容体がシナプスから取り除かれる機構を世界で初めて明らかにしたのです。神経細胞におけるAMPA受容体の輸送メカニズムの解明は、記憶や学習の“本質”に迫る発見であり、世界中の注目を集めました。
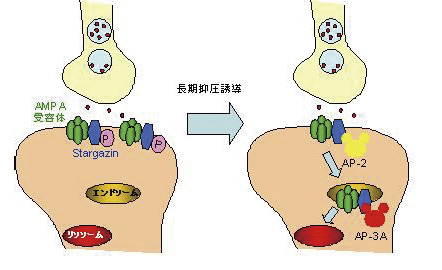
- LTD時、細胞表面のAMPA受容体の数が減少する仕組み
シナプス可塑性の理解は格段に進みました。しかし、松田准教授の興味はメカニズムの解明にとどまりません。というのは、AMPA受容体の数が制御されている機構が明らかになったことで、「シナプス可塑性を人為的に操作する」可能性が現実味を帯びてきたのです。松田准教授によれば、まだ「脳神経疾患の治療に向けた第一歩」を踏み出したばかりですが、目指しているのは、記憶や学習障害を治療する技術の開発なのです。
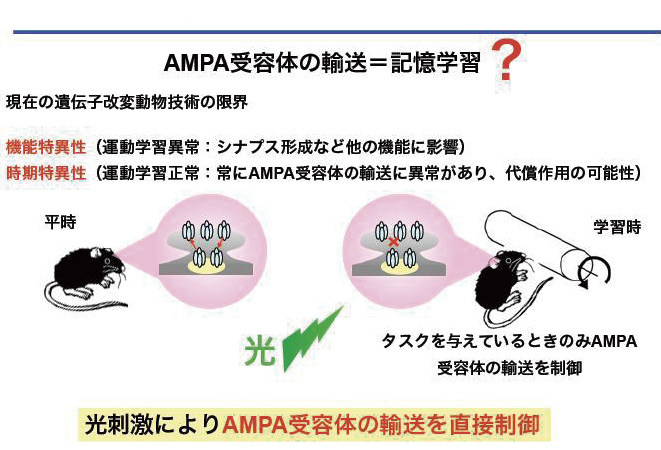
現在取り組んでいるのが、光刺激によるシナプス可塑性の制御です。AMPA受容体がうまく働かないと、記憶や学習に障害が起きることが分かっています。シナプス可塑性に重要なAMPA受容体の細胞内輸送(エンドサイトーシス)を光刺激によって阻害し、LTDの誘導を一時的に止めたマウスが、その期間だけ記憶や学習の能力が低下していれば、シナプス可塑性と記憶や学習の脳機能が、直接関連していることを示すことができます。
シナプス可塑性の制御法を開発した暁には、他の細胞内小器官の制御にもその技術を適用できるだろうと松田准教授は考えています。まず想定できるのは細胞小器官の一つであるゴルジ体で、ゴルジネットワークの機能を制御できれば、アンジェルマン症候群などのいくつかの疾患で異常をきたした神経細胞を再生できるのではないかと見通しています。より長期的には、ミトコンドリアへの展開です。光でミトコンドリアを制御できるようになれば、人工的に動物細胞に光合成を行わせることができるようになるかもしれません。
ミトコンドリアはパーキンソン病などの神経疾患との関連も深いと言われており、こうした病気の治療にも将来、道が開けることになるのでしょうか。もっとも、AMPA受容体が関与する疾患も多くあります。認知症や虚血、神経変性疾患時の神経細胞死などで、このような疾患を治療する新薬の登場も待たれます。
「研究はやればやるほど、分からないことが出てきて面白い」と話す松田准教授。「細胞内小器官の光制御システムが完成したら、どんな細胞にも使える。細胞を扱うあらゆる企業や機関に使って欲しい」と考えています。電気通信大学に2014年に新たに研究室を構えたので、工学分野との融合研究も模索しているということです。
【取材・文=藤木信穂】