【ニュースリリース】トンネル掘削をする細菌! ~細菌が極狭通路を突破する仕組みをはじめて解明~
2026.01.22
ポイント
- 極狭な通路の突破: 細菌が、約1マイクロメートル四方という、細菌1匹がぎりぎり通れるような極めて狭い通路をドリル運動により効率的に自力で通過できることを発見。
- ドリル運動: 細菌は自らの「べん毛」を細胞表面に巻き付けて、トンネル掘削機のように回転させる独特の泳ぎ方(ドリル運動)で狭い空間を推進し、方向性のある移動を実現。
- 微小流体デバイスの構築: 宿主昆虫(ホソヘリカメムシ)の腸内にある狭い共生器官通路を模倣し、約1マイクロメートル四方のチャンネルを持つ微小流体デバイスを開発。このデバイス内で共生細菌の狭小空間での運動を再現し、高速蛍光顕微鏡で可視化。
- ドリル運動の検証とモデル化: 実験と並行して物理モデルによる数値シミュレーションを行い、ドリル運動が狭い空間で推進力を高める物理的理由を解明。また、遺伝子操作によってべん毛の根元にある「フック」の柔軟性を変化させ、この柔軟性がドリル運動と感染能力に不可欠であることを証明。
概要
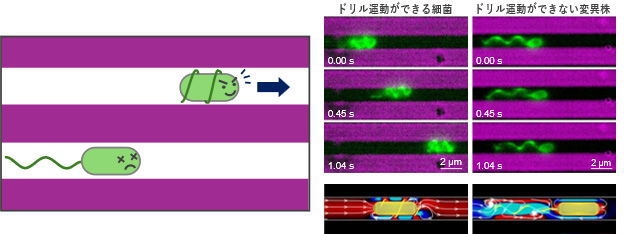
中根大介准教授(基盤理工学専攻)および菅哲朗教授(機械知能システム学専攻)、立命館大学(以下、「立命大」)の和田浩史教授、産業技術総合研究所(以下、「産総研」)の古林真衣子主任研究員・菊池義智研究チーム長らの研究グループは、細菌が自らのべん毛を細胞に巻き付けて回転させることで、"トンネル掘削機"のように幅1マイクロメートル程度の極めて狭い通路を突破できることを発見しました(図左)。研究チームは昆虫の腸内にある共生細菌の通り道を再現した微小流体デバイスを構築し、極狭通路では細菌がドリル運動をする頻度が大幅に増加することを発見しました。またシミュレーションや遺伝子操作実験により、このドリル運動が狭小空間で推進力を生む仕組みと、べん毛の基部の柔軟性がドリル運動に重要な役割を果たすことを突き止めました。本研究成果は、細菌が狭い環境を乗り越える新たな運動戦略を示したものであり、国際学術誌「Nature Communications」に掲載されました。
背景
自然界の微生物が暮らす環境には、土壌中の細孔や動植物体内の管腔など、微小で閉ざされた"極狭通路"が数多く存在します。動物と微生物の共生の中には、宿主が狭窄部と呼ばれる極めて細い通路を作り、共生に適した細菌だけを奥の器官へ通過させる例があります。例えば、農業害虫であるホソヘリカメムシの消化管には直径約1マイクロメートルの細い管状の構造が存在し、環境中の特定の共生細菌のみがそこを通り抜けて腸内の共生器官へ到達します( 産総研プレスリリース2015年9月1日)。しかし、そのような極狭通路をどのようにして細菌が通過するのか、そのメカニズムは不明でした。
近年、このホソヘリカメムシの共生細菌(Caballeronia insecticola)において、通常の運動「べん毛を後方にたなびかせて泳ぐ」様式に加え、「べん毛を前方で自分の体に巻き付けて泳ぐ」様式が報告されました(学習院大学・産総研共同プレスリリース2017年12月25日)。しかし、このようなべん毛巻き付き運動が狭い空間でどのような利点をもたらすのか、その生態学的意義は十分には検証されていませんでした。
手法
研究グループは、微小流体デバイスと呼ばれる微細加工技術を用いたモデル装置を製作しました。この装置は高さ・幅とも約1マイクロメートル程度(1ミリメートルの 1/1,000の大きさ)の極狭通路を有し、カメムシの腸内にある狭窄部を再現しています。このデバイス内で共生細菌が移動するとき、べん毛繊維を蛍光標識して可視化し、蛍光顕微鏡で撮影しました。また、この巻き付き泳法の物理的原理を探るため、細菌を狭い筒状空間内で泳がせる物理シミュレーションを実施しました。さらに、遺伝子操作により細菌のべん毛フックを改変する実験も行いました。具体的には、ドリル運動細菌(C.insecticola)と非ドリル運動細菌(近縁のBurkholderia anthina)との間でべん毛フックと呼ばれる部分の遺伝子を交換した変異株を作製し、フックの柔軟性が運動に及ぼす影響と、昆虫への感染効率への影響を評価しました。本学が光学顕微鏡観察とデバイス作製、立命大・東北大が物理モデルの構築、産総研・秋田県立大が遺伝子解析を担当しました。
成果
微小流体デバイス内で観察した結果、共生細菌は極狭通路でべん毛を高頻度で巻き付け、巻き付いたべん毛を回転させることでスムーズに前進する様子が捉えられました(図右上)。一方、通常の広い空間では同じ細菌でもべん毛を巻き付ける頻度は低く、べん毛を後方になびかせて泳ぐ頻度が高くなっていました。つまり、空間の狭さそのものが細菌のドリル運動を誘発することが示されました。微小流体デバイス内では、共生細菌の約65%が巻き付き状態で泳ぐのに対し、開放的な標準チャンバー内ではその割合が15%程度と大きな差がみられました。さらに別種の細菌についても調べたところ、狭い環境下でドリル運動を行う種(例えばPandoraea属の一部)では移動速度がほとんど低下しないのに対し、ドリル運動ができない種では狭い空間に入ると著しく遊泳速度が低下することが明らかになりました。
物理シミュレーションの結果、狭い空間ではべん毛を伸ばしたままでは周囲の液体をうまく後方へ押し出せないことが示されました(図右下)。一方、べん毛を細胞に巻き付けた状態では、液体を掻き出しながら前進する流れが発生していました。これは、狭い隙間では壁との摩擦で流体が停滞しやすく、通常のべん毛運動ではほとんど推進力を生み出せないのに対し、ドリル運動では巻き付けたべん毛は壁との隙間をねじ込むように流体を動かして推進力に変えているためです。実際に、ドリル運動は極狭通路では速度低下がほとんど見られず、広い空間での通常遊泳と同程度の速度で前進できることが確認されました。
遺伝子改変実験では、ドリル運動細菌(C. insecticola)の柔らかいフックを、非ドリル細菌(B. anthina)の少し硬いフックへと交換したところ、極狭通路でべん毛を巻き付けられなくなり、移動距離はほぼゼロに低下しました。逆に非ドリル運動細菌の少し硬いフックを、ドリル細菌由来の柔らかいフックへと交換すると、チャンネル内で部分的にではあるものの巻き付き泳法が現れ、移動距離も増加しました。このようなフックの硬さがドリル運動に重要であることは、物理シミュレーションでも再現できました。さらに、フックを硬くしたドリル運動細菌は、宿主カメムシへの感染競争力(共生器官へ定着する能力)が大幅に低下することも判明しました。これらの結果から、べん毛フックの柔軟性が巻き付き運動の鍵であり、狭小空間での移動効率、ひいては宿主への感染成功率が左右されることが実証されました。
今後の期待
本研究では、ドリル運動は細菌が極狭通路を突破するために進化させた巧みな移動戦略であることを示しました。この知見により、これまで不明だった微小空間における細菌の行動原理や、宿主-共生菌間の相互作用のメカニズムが解明に近づくことが期待されます。特に、本研究で対象とした昆虫共生菌だけでなく、病原細菌であるカンピロバクターやヘリコバクター、緑膿菌などでもドリル運動が報告されており、粘液層や腸陰窩のような粘性が高く狭い領域で宿主体内へ侵入・定着する普遍的な戦略である可能性があります。したがって、この運動を阻害あるいは促進することで、害虫防除や病原菌感染の制御につながる応用も考えられます。また、微生物が持つ巧みな運動様式は、マイクロマシンやナノロボット開発などへの着想を与える可能性もあり、生物模倣技術の観点からも注目されます。今後、本研究で開発した微小流体デバイスを応用して土壌や生体内など様々な狭小環境での微生物の振る舞いを調べることで、環境中の細菌生態や共生システムの解明が一層進むことが期待されます。
(論文情報)
掲載誌:Nature Communications
タイトル:Bacteria break through one-micrometer-square passages by flagellar wrapping
著者:Aoba Yoshioka, Yoshiki Y. Shimada, Toshihiro Omori, Naoki A. Uemura, Kazutaka Takeshita, Kota Ishigami, Hiroyuki Morimura, Maiko Furubayashi, Tetsuo Kan, Hirofumi Wada, Yoshitomo Kikuchi, Daisuke Nakane
論文URL: https://doi.org/10.1038/s41467-025-67507-9
DOI:10.1038/s41467-025-67507-9
公表日:2026年1月22日(木)
(外部資金情報)
本研究は、JSPS 科学研究費補助金 学術変革領域研究(B)微生物が動く意味(22H05066, 22H05067, 22H05068)、JST創発的研究支援事業(JPMJFR2411)の支援を受けたものです。
詳細はPDFでご確認ください。
